Urso
As Informações Neste Site Não Constituem Aconselhamento Médico. Não Vendemos Nada. A Precisão Da Tradução Não É Garantida. Isenção De Responsabilidade
Resumo das drogas
O que é urso?
Urso (ursodiol) é um até ácido usado para tratar pequenos cálculos biliares em pessoas que não podem ter vesícula biliar cirurgia e para evitar cálculos biliares em pacientes com excesso de peso submetidos a uma rápida perda de peso. O URSO também é usado para tratar a cirrose biliar primária (PBC). URSO está disponível em genérico forma.
Quais são os efeitos colaterais do URSO?
Urso
Pílulas de liberação instantânea de 30 mg de oxicodona
- náusea
- dor no estômago superior
- coceira
- sentimento cansado
- perda de apetite
- urina escura
- fezes cor de argila
- amarelecimento da pele ou olhos
- fraqueza repentina ou sentimento doente
- febre
- calafrios
- dor de garganta
- feridas na boca
- Ferida da pele e
- problema de engolir
Obtenha ajuda médica imediatamente se tiver algum dos sintomas listados acima.
Os efeitos colaterais comuns do URSO incluem:
- dor de estômago ou dor
- náusea
- diarréia
- constipação
- tontura
- sentimento cansado
- dor nas costas
- perda de cabelo
- dor de cabeça
- febre
- calafrios
- dores no corpo
- sintomas da gripe
- escorrendo ou nariz entupido
- tosse ou
- sintomas de frio.
Diga ao seu médico se você tem efeitos colaterais improváveis, mas graves do URSO, incluem:
- fraqueza
- inchaço dos tornozelos ou pés
- aumento da sede ou micção
- sinais de infecção (por exemplo, febre persistente dor de garganta) ou
- Sangramento ou hematoma fácil.
Procure cuidados médicos ou ligue para o 911 de uma só vez, se tiver os seguintes efeitos colaterais graves:
- Sintomas graves oculares, como perda súbita de visão de visão, visão de visão da visão ou inchaço ou vendo halos ao redor das luzes;
- Sintomas cardíacos graves, como batimentos cardíacos irregulares ou batendo rápidos; flutuando no seu peito; falta de ar; e tontura repentina Tardete ou desmaiar;
- Confusão de dor de cabeça grave arborizada braço de fala ou fraqueza da perna TROBLEMENTO A perda de coordenação sentindo músculos instáveis muito rígidos, febre alta, sudorese ou tremores.
Este documento não contém todos os efeitos colaterais possíveis e outros podem ocorrer. Verifique com seu médico para obter informações adicionais sobre efeitos colaterais.
Dose para urso
A dose de adulto recomendada para URSO no tratamento do PBC é de 13 a 15 mg/kg/dia administrado em duas a quatro doses divididas com alimentos. O regime de dosagem deve ser ajustado de acordo com a necessidade de cada paciente, a critério do médico.
Quais drogas substâncias ou suplementos interagem com o URSO?
O URSO pode interagir com os estrogênios de colestiramina colestipol (pílulas anticoncepcionais ou substituição de hormônios) ou antiácidos que contêm alumínio (como Rolaids Mylanta ou Maalox). Diga ao seu médico todos os medicamentos que você está tomando.
Urso durante a gravidez ou amamentação
Durante a gravidez, o URSO deve ser usado apenas quando prescrito. Não se sabe se esse medicamento passa para o leite materno. Consulte seu médico antes de amamentar.
Informações adicionais
Nosso Centro de Medicamentos de Efeitos Laterais URSO (Ursodiol) fornece uma visão abrangente das informações disponíveis dos medicamentos sobre os possíveis efeitos colaterais ao tomar este medicamento.
Informações sobre medicamentos da FDA
- Descrição do medicamento
- Indicações
- Efeitos colaterais
- Avisos
- Overdose
- Farmacologia Clínica
- Guia de medicação
Descrição para urso
O URSO 250 (Ursodiol 250 mg) está disponível como um comprimido revestido de filme para administração oral. O URSO Forte (Ursodiol 500 mg) está disponível como um comprimido revestido de filme para administração oral. O ursodiol (UDCA de ácido ursodeoxicólico) é um ácido biliar de ocorrência natural encontrado em pequenas quantidades na bile humana normal e em quantidades maiores nos biles de certas espécies de ursos. É um pó branco de sabor amargo que consiste em partículas cristalinas livremente solúveis em etanol e ácido acético glacial ligeiramente solúvel em clorofórmio com moderação em éter e praticamente insolúvel em água. O nome químico de Ursodiol é 3α7ß-di-hidroxi-5ß-cholan-24-OIC (C24H40O4). O ursodiol tem um peso molecular de 392,56. Sua estrutura é mostrada abaixo.
 |
Ingredientes inativos: celulare microcristalina Poveidona amido de sódio Glicolato Estearato estearato Etilcelulose dibutil sebacato Carnauba Cera hidroxipropilmetilcelululose PEG 3350 PEG 8000 Cetílico álcool liurinlfato e hidrogênio.
Usos para urso
Os comprimidos URSO 250 e URSO Forte (Ursodiol) são indicados para o tratamento de pacientes com colangite biliar primária (PBC).
Dose para urso
Informações gerais de dosagem
A dose de adulto recomendada para URSO 250 e URSO Forte no tratamento de PBC é de 1315 mg/kg/dia administrado em duas a quatro doses divididas com alimentos. O regime de dosagem deve ser ajustado de acordo com a necessidade de cada paciente a critério do médico.
Testes de função hepática
Testes de função hepática (γ-GT alcalina fosfatase AST ALT) e os níveis de bilirrubina devem ser monitorados todos os meses durante três meses após o início da terapia e a cada seis meses depois [veja Avisos e precauções ].
Marcando o tablet URSO Forte
O comprimido URSO Forte pode ser quebrado a metades para fornecer dosagem recomendada.
Para quebrar o comprimido Urso Forte, coloque facilmente o comprimido em uma superfície plana com a seção pontuada por cima. Segure o tablet com os polegares colocados perto da parte marcada do tablet (ranhura). Em seguida, aplique pressão suave e afaste os segmentos do tablet (os segmentos quebrando incorretamente não devem ser usados). Os segmentos devem ser lavados, sem water, com a água que mantém os segmentos na boca pode revelar um sabor amargo. Devido aos segmentos de sabor amargo, devem ser armazenados separadamente de comprimidos inteiros. [ver Como fornecido / Armazenamento e manuseio ].
Como fornecido
Formas e forças de dose
- Urso 250 : 250 mg comprimido
- URSO Forte : 500 mg de tablet pontuado
Armazenamento e manuseio
Urso 250
Cada URSO 250 comprimido elíptico de filme biconvexo branco gravado com URS785 contém 250 mg de ursodiol. Disponível em garrafas de 100 comprimidos ( NDC 58914-785-10).
URSO Forte
Cada urso forte elíptico biconvexo marcou comprimido com revestimento de filme gravado com URS790 contém 500 mg de ursodiol. Disponível em garrafas de 100 comprimidos ( NDC 58914-79010). Armazene a 20 ° C a 25 ° C (68 ° F a 77 ° F). Dispense em um recipiente apertado.
Meias tablete (URSO pontuado Forte 500 mg de comprimidos quebrados ao meio) Mantenha a qualidade aceitável por até 28 dias quando armazenados na embalagem atual (garrafas) a 20 ° C a 25 ° C (68 ° F a 77 ° F). Devido ao sabor amargo, os segmentos pela metade devem ser armazenados separadamente de todos os comprimidos [veja Dosagem e administração ].
Distribuído por: Allergan USA Inc. Madison NJ 07940 www.allergan.com. Revisado: maio de 2021
Efeitos colaterais para o URSO
Experiência em estudos clínicos
Como os ensaios clínicos são conduzidos sob condições amplamente variadas, as taxas de reação adversa observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparados às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática clínica.
A tabela a seguir resume as reações adversas observadas em dois ensaios clínicos controlados por placebo.
| Reações adversas | Visita aos 12 meses | Visita aos 24 meses | ||
| Udca n (%) | Placebo n (%) | Udca n (%) | Placebo n (%) | |
| Diarréia | ---- | ---- | 1 (1,32) | ---- |
| Creatinina elevada | ---- | ---- | 1 (1,32) | ---- |
| Glicose no sangue elevado | 1 (118) | ---- | 1 (1,32) | ---- |
| Leucopenia | ---- | ---- | 2 (2.63) | ---- |
| Úlcera péptica | ---- | ---- | 1 (1,32) | ---- |
| Erupção cutânea | ---- | ---- | 2 (2.63) | ---- |
| Trombocitopeni a | ---- | ---- | 1 (1,32) | ---- |
| Nota: As reações adversas que ocorrem na mesma ou maior incidência no placebo, como no grupo UDCA, foram excluídas desta tabela (isso inclui diarréia e trombocitopenia aos 12 meses de náusea/febre de vômito e outras toxicidade). UDCA = ácido ursodeoxicólico = ursodiol |
Em um estudo cruzado randomizado em sessenta pacientes com PBC, sete pacientes (11,6%) relataram nove reações adversas: dor abdominal e astenia (1 paciente) náusea (3 pacientes) dispepsia (2 pacientes) e anorexia e esofagite (1 paciente cada). Um paciente no regime duas vezes por dia (dose total de 1000 mg) retirou -se devido a náusea. Todas essas nove reações adversas, exceto esofagite, foram observadas com o regime duas vezes por dia em uma dose diária total de 1000 mg ou superior. No entanto, uma reação adversa pode ocorrer em qualquer dose.
Experiência de pós -mercado
The following adverse reactions presented by system organ class in alphabetical order have been identified during post approval use of ursodiol. Because these reactions are reported voluntarily from a population of uncertain size it is not always possible to reliably estimate their frequency or establish a causal relationship to drug exposure.
- Distúrbios gastrointestinais: Desconforto abdominal Constipação de dor abdominal Diarréia DiRepsia Náusea Vômito.
- Distúrbios gerais e condições do local da administração: Malaise Edema Periférico Pirexia.
- Distúrbios hepatobiliares: icterícia (ou agravamento de icterícia pré-existente).
- Distúrbios do sistema imunológico: Hipersensibilidade às drogas para incluir edema facial urticária angioedema e edema laríngeo.
- Testes de laboratório anormais: O ALT aumentou o aumento da fosfatase alcalina no sangue aumentou o aumento da bilirrubina γ-GT aumentou a enzima hepática aumentada no teste de função hepática transaminases anormais aumentadas.
- Distúrbios musculoesqueléticos e conjuntivos do tecido: mialgia
- Distúrbios do sistema nervoso: tontura dor de cabeça.
- Distúrbios torácicos e mediastinais respiratórios: tosse.
- Pele e transtorno de tecido subcutâneo: Alopecia prurido erupção cutânea.
Interações medicamentosas para URSO
Agentes de sequência de ácido biliar
Até Agentes de sequestro ácido, como colestiramina e colestipol, podem interferir na ação do URSO 250 e URSO Forte, reduzindo sua absorção.
Antiácidos à base de alumínio
Demonstrou-se que os antiácidos à base de alumínio adsorve os ácidos biliares in vitro e podem ser esperados que interfiram no URSO 250 e URSO Forte da mesma maneira que os agentes de sequência de ácido biliar.
Que tipo de medicamento é codeína
Drogas que afetam o metabolismo lipídico
Estrógenos contraceptivos orais e clofibrato (e talvez outros medicamentos para baixar lipídios) aumentam a secreção de colesterol hepática e incentivam a formação de cálculos biliares de colesterol e, portanto, podem neutralizar a eficácia do URSO 250 e do URSO Forte.
AVISOS PARA URSO
Incluído como parte do PRECAUÇÕES seção.
Precauções para o URSO
Pacientes com encefalopatia hepática de sangramento variceal ascite ou necessitando de um transplante de fígado urgente devem receber tratamento específico adequado.
Testes de função hepática anormal
Os testes de função hepática (γ-GT alcalina fosfatase AST ALT) e os níveis de bilirrubina devem ser monitorados todos os meses durante três meses após o início da terapia e a cada seis meses depois. Esse monitoramento permitirá a detecção precoce de uma possível deterioração da função hepática. Treatment discontinuation should be considered if the above parameters increase to a level considered clinically significant in patients with stable historical liver function test levels.
Cuidado deve ser exercido para manter o fluxo biliar dos pacientes que tomam ursodiol.
Toxicologia não clínica
Carcinogênese mutagênese comprometimento da fertilidade
Em dois estudos de carcinogenicidade oral de 24 meses em camundongos ursodiol em doses de até 1000 mg/kg/dia (3000 mg/m²/dia) não foram tumorigênicas. Com base na área da superfície corporal para uma pessoa de 50 kg de altura média (área da superfície corporal de 1,46 m²), essa dose representa 5,4 vezes a dose clínica máxima recomendada de 15 mg/kg/dia (555 mg/m²/dia).
Em um estudo de carcinogenicidade oral de dois anos em Fischer 344 ratos ursodiol em doses de até 300 mg/kg/dia (1800 mg/m²/dia 3,2 vezes a dose humana máxima recomendada com base na área da superfície corporal) não foi tumorigênica.
Em um estudo de carcinogenicidade oral de um vencedor (126-138 semanas), os ratos Sprague-Dawley foram tratados com doses de 33 a 300 mg/kg/dia 0,4 a 3,2 vezes a dose humana máxima recomendada com base na área da superfície corporal. Ursodiol produziu um significativamente (p<0.5 Fisher's exact test) increased incidence of pheochromocytomas of the adrenal medulla in females of the highest dose group.
Em estudos de carcinogenicidade oral de 103 semanas de ácido litocólico, um metabólito de doses de ursodiol até 250 mg/kg/dia em camundongos e 500 mg/kg/dia em ratos não produziram tumores. Em um estudo de ratos de 78 semanas, a instilação intrarretal do ácido litocólico (1 mg/kg/dia) por 13 meses não produziu tumores colorretais. Um efeito promotor de tumor foi observado quando foi administrado após uma única dose intrarretal de um conhecido carcinogênio n-metil-n'-nitro-n-nitrosoguanidina. Por outro lado, em um estudo de ratos de 32 semanas, ursodiol em uma dose diária de 240 mg/kg (1440 mg/m² 2,6 vezes a dose humana máxima recomendada com base na área da superfície corporal) suprimiu o efeito carcinogênico de outro carcinogênio conhecido.
Ursodiol was not genotoxic in the Ames test the mouse lymphoma cell (L5178Y TK /-) forward mutation test the human lymphocyte sister chromatid exchange test the mouse spermatogonia chromosome aberration test the Chinese hamster micronucleus test and the Chinese hamster bone marrow cell chromosome aberration test.
Ursodiol em doses orais de até 2700 mg/kg/dia (16200 mg/m²/dia 29 vezes a dose humana máxima recomendada com base na área da superfície corporal) não tem efeito no desempenho da fertilidade e reprodução de ratos machos e fêmeas.
Use em populações específicas
Gravidez
Resumo do risco
Dados publicados disponíveis sobre o uso de ursodiol em mulheres grávidas derivadas de estudos observacionais de ensaios clínicos randomizados e séries de casos coletadas ao longo de várias décadas não identificaram um risco associado a medicamentos de defeitos congênitos principais ou outros resultados maternos ou fetais adversos. A maioria das exposições relatadas ao Ursodiol ocorreu no segundo e terceiro trimestre da gravidez. Nos estudos de reprodução de animais, o ursodiol não teve efeitos adversos no desenvolvimento embrionário-fetal quando administrado em doses maiores que as doses terapêuticas humanas (ver Dados ).
O risco de fundo estimado de principais defeitos congênitos e aborto para a população indicada é desconhecida. Todas as gestações têm um risco de perda de defeitos congênitos ou outros resultados adversos. Na população geral dos EUA, o risco estimado de antecedentes de defeitos congênitos e aborto nas gestações clinicamente reconhecidas é de 2 a 4% e 15 a 20%, respectivamente.
Dados
Dados de animais
Não foram observados efeitos adversos no desenvolvimento do embrio-fetal com a administração oral de ursodiol em ratos e coelhos grávidas durante a organogênese em doses de até 22 e 7 vezes, respectivamente, a dose humana máxima recomendada (com base na área da superfície corporal).
sou humumy
Lactação
Resumo do risco
O ursodiol está naturalmente presente no leite humano. Não há relatos de efeitos adversos do ursodiol na criança amamentada, mas os relatórios são extremamente limitados. Não há dados sobre os efeitos do ursodiol na produção de leite. Os benefícios de desenvolvimento e saúde da amamentação devem ser considerados junto com a necessidade clínica da mãe de URSO 250 e URSO Forte e quaisquer possíveis efeitos adversos na criança amamentada do URSO 250 e URSO Forte ou da condição materna subjacente.
Uso pediátrico
A segurança e a eficácia de URSO 250 e URSO Forte em pacientes pediátricos não foram estabelecidos.
Overdose Information para URSO
Não houve relatos de superdosagem acidental ou intencional com Ursodiol. Doses orais únicas de ursodiol a 10 g/kg em camundongos e cães e 5 g/kg em ratos não eram letais. Uma dose oral única de ursodiol a 1,5 g/kg foi letal em hamsters. Os sintomas de toxicidade aguda foram salivação e vômito em cães e ataxia dispnéia ptose convulsões e coma em hamsters.
Contraindications for Urso
Pacientes com obstrução biliar completa e hipersensibilidade ou intolerância conhecidas ao Ursodiol ou a qualquer um dos componentes da formulação.
Farmacologia Clínica for Urso
Mecanismo de ação
Ursodiol A ácido biliar hidrofílico que ocorre naturalmente derivado do colesterol está presente como uma fração menor do pool de ácido biliar humano total. A administração oral de Ursodiol aumenta essa fração de maneira relacionada à dose para se tornar o principal ácido biliar que substitui/deslocando concentrações tóxicas de ácidos biliares hidrofóbicos endógenos que tendem a se acumular na doença hepática colestática. In addition to the replacement and displacement of toxic bile acids other mechanisms of action include cytoprotection of the injured bile duct epithelial cells (cholangiocytes) against toxic effects of bile acids inhibition of apotosis of hepatocytes immunomodulatory effects and stimulation of bile secretion by hepatocytes and cholangiocytes.
Farmacodinâmica
O ácido litocólico quando administrado cronicamente aos animais causa lesão hepática colestática que pode levar à morte por insuficiência hepática em certas espécies incapazes de formar conjugados de sulfato. O Ursodiol é 7-desidroxilado mais lentamente que o chenodiol. Para doses equimolares de Ursodiol e Chenodiol, os níveis de estado estacionário de ácido litocólico em ácidos biliares biliares são mais baixos durante a administração de Ursodiol do que com a administração de Chenodiol. Humanos e chimpanzés podem sulfato de ácido litocólico. Embora a lesão hepática não tenha sido associada à terapia com ursodiol, pode existir uma capacidade reduzida de sulfato em alguns indivíduos.
Farmacocinética
O Ursodiol (UDCA) está normalmente presente como uma fração menor dos ácidos biliares totais em humanos (cerca de 5%). Após a administração oral, a maioria do Ursodiol é absorvida pela difusão passiva e sua absorção é incompleta. Uma vez absorvido, o Ursodiol sofre extração hepática na extensão de cerca de 50% na ausência de doença hepática. À medida que a gravidade da doença hepática aumenta a extensão da extração diminui. No fígado, o ursodiol é conjugado com glicina ou taurina e então secretada na bile. Esses conjugados de Ursodiol são absorvidos no intestino delgado por mecanismos passivos e ativos. Os conjugados também podem ser desconjugados no íleo por enzimas intestinais, levando à formação de Ursodiol livre que pode ser reabsorvido e reconegado no fígado. O ursodiol não absorvido passa para o cólon, onde é principalmente 7-desidroxilado ao ácido litocólico. Alguns ursodiol são epimerizados para o quenodiol (CDCA) através de um intermediário de 7-oxo. O chenodiol também passa por 7-desidroxilação para formar ácido litocólico. Esses metabólitos são pouco solúveis e excretados nas fezes. Uma pequena porção de ácido litocólico é reabsorvida conjugada no fígado com glicina ou taurina e sulfatada na posição 3. Os conjugados de ácido litocólico sulfatados resultantes são excretados na bile e depois perdidos nas fezes.
Em indivíduos saudáveis, pelo menos 70% do ursodiol (não conjugado) está ligado à proteína plasmática. Nenhuma informação está disponível sobre a ligação do Ursodiol conjugado à proteína plasmática em indivíduos saudáveis ou pacientes com PBC. Seu volume de distribuição não foi determinado, mas espera -se que seja pequeno, uma vez que o medicamento é distribuído principalmente no bile e intestino delgado. O ursodiol é excretado principalmente nas fezes. Com o tratamento, a excreção urinária aumenta, mas permanece inferior a 1%, exceto em doença hepática colestática grave.
Durante a administração crônica de Ursodiol, torna -se um grande ácido biliar e plasmático biliar. Em uma dose crônica de 13 a 15 mg/kg/dia, o ursodiol constitui 30-50% dos ácidos biliares e biliares biliares.
Estudos clínicos
Eficácia do ácido ursodeoxicólico administrado a 13 a 15 mg/kg/dia em 3 ou 4 doses divididas para pacientes com PBC
Foi realizado um estudo clínico randomizado de placebo duplo-cego, multicêntrico dos EUA, para avaliar a eficácia do ácido ursodeoxicólico na dose de 13 a 15 mg/kg/dia administrada em 3 ou 4 doses divididas em 180 pacientes com PBC (78% recebidos quatro vezes por dia). Após a conclusão da porção dupla-cega, todos os pacientes entraram em uma fase de extensão de tratamento ativo de rótulo aberto.
Falha no tratamento O principal ponto final de eficácia medido durante este estudo foi definido como a necessidade de morte para a progressão histológica do transplante de fígado por dois estágios ou para o desenvolvimento da cirrose de varizes ascites ou encefalopatia marcando o desmedência da fadiga ou da incapacidade do prurido para tolerar a duplicação de drogas da bile -reta e retirada voluntária. Após dois anos de tratamento duplo-cego, a incidência de falha no tratamento foi significativamente (p<0.01) reduced in the Urso 250 mg group (20 of 86 (23%) as compared to the placebo group (40 of 86 (47%). Time to treatment failure which excluded doubling of serum bilirubin and voluntary withdrawal was also significantly (p<0.001) delayed in the URSO 250 treated group (n=86 803.8±24.9 d vs. 641.1±24.4 d for the placebo group (n=86) on average) regardless of either histologic stage or baseline bilirubin levels (>1.8 ou <1.8 mg/dL).
O uso de uma definição de falha no tratamento que excluiu a duplicação da bilirrubina sérica e o tempo de retirada voluntária para a falha do tratamento foi significativamente atrasado no grupo URSO 250. Em comparação com o tratamento com placebo com o URSO 250, resultou em uma melhora significativa nos seguintes bioquímicos hepáticos séricos quando comparado à linha de base: fosfatase alcalina e IgM total de bilirrubina sgot.
Eficácia do Ursodiol administrado a 14 mg/kg/dia como dose uma vez por dia para pacientes com PBC
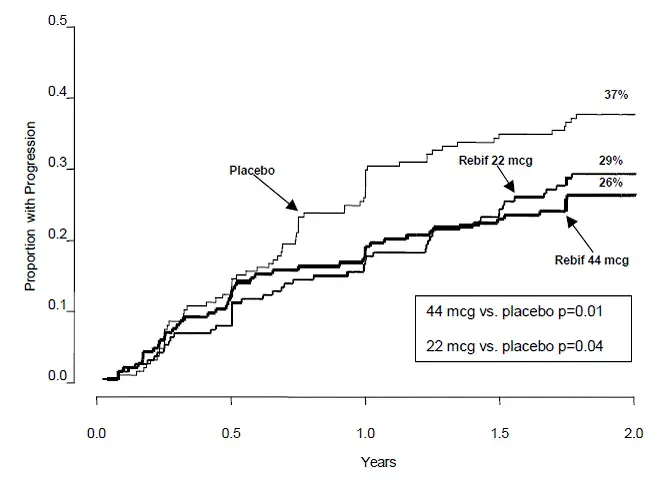
Um segundo estudo realizado no Canadá randomizou 222 pacientes com PBC para Ursodiol 14 mg/kg/dia ou placebo administrado como dose uma vez por dia de maneira dupla-cega durante um período de dois anos. Em dois anos um estatisticamente significativo (p<0.001) difference between the two treatments (n=106 for the Urso 250 group and n=106 for the placebo group) in favor of ursodiol was demonstrated in the following: reduction in the proportion of patients exhibiting a more than 50% increase in serum bilirubin; median percent decrease in bilirubin (-17.12% for the Urso 250 group vs. +20.00% for the placebo group) transaminases (-40.54% for the Urso 250 group vs. +5.71% for the placebo group) and alkaline phosphatase (-47.61% for the Urso 250 group vs. -5.69% for the placebo group); incidence of treatment failure; and time to treatment failure. The definition of treatment failure included: discontinuing the study for any reason; a total serum bilirubin level greater than or equal to 1.5 mg/dl or increasing to a level equal to or greater than two times the baseline level; and the development of ascites or encephalopathy. Evaluation of patients at 4 years or longer was inadequate due to the high drop-out rate (n=10 withdrew from the Urso 250 group vs. n=15 from the placebo group) and small number of patients. Therefore death need for liver transplantation histological progression by two stages or to cirrhosis development of varices ascites or encephalopathy marked worsening of fatigue or pruritus inability to tolerate the drug doubling of serum bilirubin and voluntary withdrawal were not assessed.
Eficácia do URSO 250 administrado duas vezes ao dia, versus quatro vezes ao dia, cronogramas de dosagem divididos para pacientes com PBC
Um estudo cruzado randomizado de dois períodos em cinquenta pacientes com PBC comparou a eficácia do URSO 250 (Ursodiol) em duas vezes ao dia, versus quatro vezes ao dia dividido em cronogramas de dosagem em 50 pacientes por 6 meses em cada período cruzado. Alterações percentuais médias da linha de base nos resultados dos testes hepáticos e no escore de risco de maionese (n = 46) e enriquecimento sérico com UDCA (n = 34) não foram estatisticamente significativos com qualquer dose a qualquer intervalo de tempo. Este estudo demonstrou que a UDCA (13 a 15 mg/kg/dia), dada duas vezes por dia, é igualmente eficaz para a UDCA dada quatro vezes por dia. Além disso, o URSO 250 foi dado como um único versus três vezes ao dia cronogramas de dosagem em 10 pacientes. Devido ao pequeno número de pacientes neste braço do estudo, não foi possível realizar comparações estatísticas entre esses regimes.
Informações do paciente para urso
Tratamentos apropriados
Pacientes com as seguintes condições devem ser instruídos a receber medidas de gerenciamento apropriadas: encefalopatia hepática de sangramento variceal ascites que precisam de um transplante de fígado urgente ou deterioração da função hepática [ver [ver Avisos e precauções ].
Cuidado deve ser exercido para manter o fluxo biliar dos pacientes que tomam ursodiol.
Interações medicamentosas
Os pacientes devem ser informados de que a absorção de URSO 250 e URSO Forte pode ser reduzida se estiverem tomando agentes de sequestradores de ácido biliar, como colestiramina e antiácidos à base de alumínio ou medicamentos à base de alumínio, conhecidos por alterar o metabolismo do colesterol [veja Interações medicamentosas ].